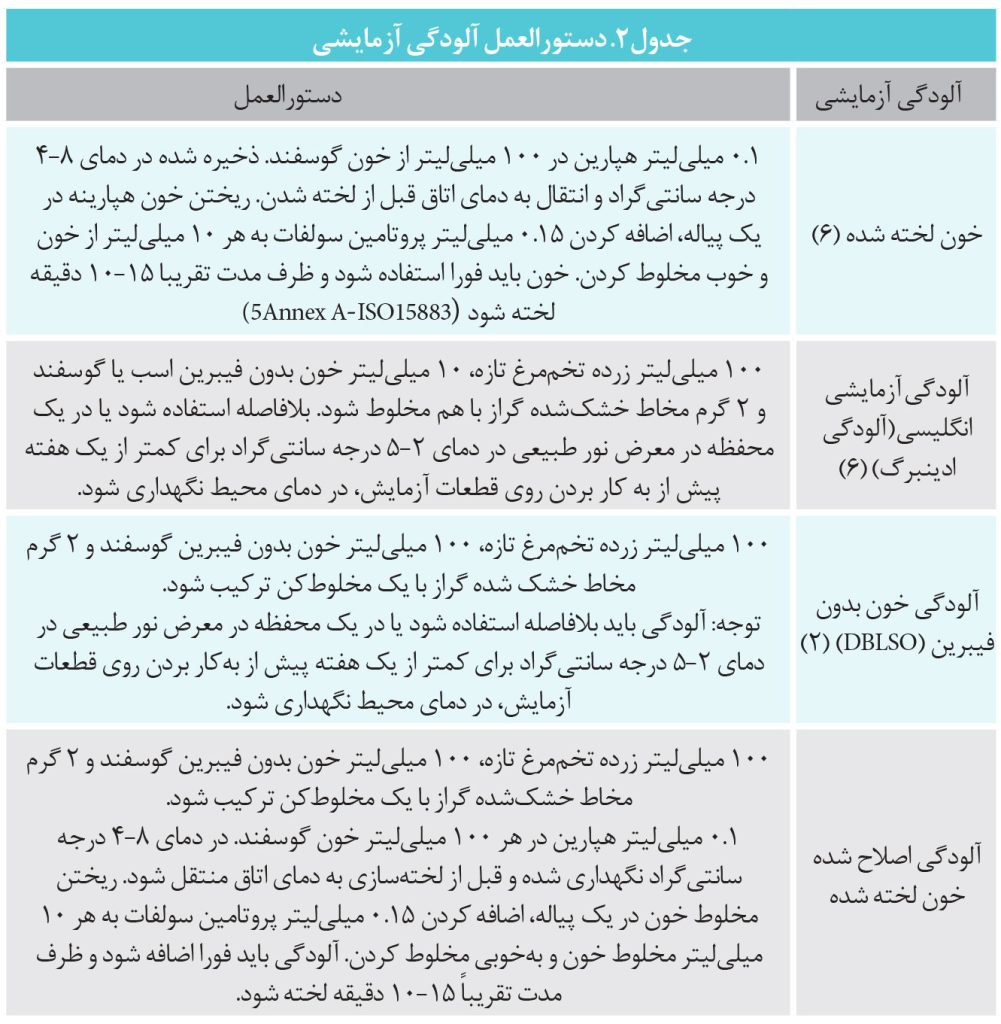
مقایسه میزان چسبندگی مواد آلاینده آزمایشی:پاکسازي يکي از بخشهاي ضروري در استريليزاسيون ابزارهاي پزشکي چندبار مصرف است. بنابراين، مطالعات اعتبارسنجي قدرتمندي مورد نياز است تا کفايت دستورالعملهاي پاکسازي، براي آلودگيهاي بيولوژيک و شيميايي را تضمين کند. فاکتور مهم در اين مطالعات اعتبارسنجي، انتخاب و استفاده آلودگيهاي نمونه آزمايشي است. آلودگيهاي آزمايشي بايد خصوصياتي شبيه آلودگي هنگام استفاده باليني از ابزارها باشند. موادي که براي شبيهسازي وجود دارد انديکاتورهاي شستشو، تست پروتئين و تست خون ناميده ميشوند. اين تستها بايد چسبناکي و انحلالپذيري روي ابزار شبيه آلودگي واقعي داشته باشند.
اين مطالعه چهار مورد از آلودگيهاي آزمايشي که توسط استانداردهاي ISO و ASTM براي جراحي عمومي و يا ارتوپدي مناسب تشخيص داده شدهاند را مقايسه ميکند و نتيجه بهدست آمده نشان ميدهد که DBLSO* (نماينده آلودگي در جراحي ارتوپدي)، نسبت به خون لخته شده BLSO*، (نماينده آلودگي جراحي عمومي) شرايط بهتري دارد. اين مطالعه همچنين نشان داد که اگر آلودگي ادينبرگ براي ابزارهاي جراحي عمومي يا ارتوپدي، به منظور شبيهسازي اعتبارسنجي پاکسازي به شکل يکسان استفاده شود، ممکن است چالش بزرگي را ايجاد کند.
■ Defibrinated Blood Soilخوني که پروتئين فيبرين آن جدا شده است.
■ Blood Soil خون خشکشده با پروتئين فيبرين است. (مطالعه بيشتر شود. مترجم)
■ آلودگي ادينبرگ : محصولي که از خون اسب بدون پروتئين فيبرين تهيه ميشود.
کليد واژهها
- آلودگي
- پاکسازي
- پروتئين
- چسبناکي
- چسبندگي
- انحلالپذيري
- جراحي
- ابزار جراحي
مقدمه
شرکتهاي توليدکننده ابزارهاي جراحي تعيين ميکنند که ابزارهاي پزشکي چندبار مصرف براي استريل مجدد مناسب هستند. هنگام استفاده باليني، ممکن است اين ابزارها در معرض آلودگيهاي شيميايي و بيولوژيک قرار گيرند و سطح بالاي پروتئين، کربوهيدرات و چربي بافتها و مايعات بدن آنها را آلوده کند. شرکتها، براي تدوين دستورالعملهاي استريل مرتبط با ابزار (IFU) از آلودگيهاي آزمايشي به منظور شبيهسازي آلودگي سطوح استفاده ميکنند. در انتخاب يک آلودگي آزمايشي مناسب، بايد سختترين نوع آلودگي وسيله، طي استفاده باليني درنظر گرفته شود تا بتوان مخلوطي از اجزاء مانند ترشحات انساني، خون، بافت و تکهها/تراشههاي استخواني را شبيهسازي کرد.
انتخاب آلودگي آزمايشي مناسب براي مطالعات ميزان اثربخشي پاکسازي بايد علمي و مستند بوده و برگرفته از يک بازنگري اصولي يا نشاندهنده تناسب آن براساس کاربرد باليني ابزار جراحي باشد. اين انتخاب ممکن است بر پايه اين موارد باشد: تماس با بيمار يا نوع استفاده از آن، ترکيبات آن و غلظت محتويات آلودگي آزمايشي و ويژگيهاي فيزيکي آن.
تماس با بيمار يا روش استفاده از ابزار و انواع آلودگيهاي باليني که وسيله با آنها مواجه ميشود، بايد مدنظر قرار داده شود. براي مثال، تماس با خون طي استفاده باليني (مخصوصا جراحي) يک رويداد رايج است، بنابراين براي ابزارهايي که با خون تماس دارند، آلودگي آزمايشي شبيهسازيشده بايد بر پايه خون باشد و غلظت آن نشاندهنده سطوح خوني باقي مانده پس از تماس با بيمار باشد. ترکيب آلودگي آزمايشي بايد نشاندهنده محتملترين ترکيباتي باشد که اين وسيله ممکن است در بدترين وضعيت باليني در معرض آن قرار گيرد. مثالهاي اين ترکيبات در جدول 1 آمده است.
فرمولاسيون آلودگي آزمايشي بايد نشاندهنده غلظت شناساگر (مانند پروتئين) موجود روي وسيله، پس از استفاده باليني باشد. غلظت شناساگر بايد به روش کمّي قابل اندازهگيري باشد (غلظت پروتئين مورد نظر بايد قابل مقايسه با سطوح غلظت پروتئين باليني باشد و از طريق يک روش معتبر بررسي پروتئين باقي مانده، قابل اندازهگيري باشد). آلودگي آزمايشي ويژگيهاي فيزيکي (مانند چسبناکي، چسبندگي و انحلالپذيري در آب) دارد که ميتواند روي نتيجه مطالعه اثربخشي پاکسازي تأثير داشته باشد.
چسبناکي [ويسکوزيته (ميزان لزج بودن)] ميزان مقاومت در برابر جريان يافتن مواد است.
اين مورد فاکتور مهمي در انتخاب آلودگي آزمايشي بهعنوان مادهاي که مايعات زيستي بدن در زمان برخورد با ابزار جراحي را شبيه سازي ميکند، بايد درنظر گرفته شود. براي مثال، ممکن است بخشي از خون را دربرگيرد. تشکيل ترومبين، آنزيمي در پلاسماي خون که از طريق تبديل فيبرينوژن به فيبرين سبب لخته شدن خون ميشود، در شرايط ويسکوزيته بالا، افزايش مييابد. چسبندگي، عمل يا فرآيند چسبيدن به يک سطح يا شئ، ويژگي فيزيکي ديگري از آلودگي است که مشخص ميکند آلودگي چگونه به سطح مواد يا برجستگيهاي ابزار متصل ميشود. افزايش چسبندگي با دشواري برداشتن آلودگي از روي وسيله مرتبط است. مشخص شده، آلودگيهايي که جزئي از زرده تخممرغ را دارند، به دليل اختلاط خاص با پروتئينها، کربوهيدراتها و چربيها، سختترين وضعيت را در برداشتن دارند. در عوض، مشخص شده آلودگيهايي که فقط حاوي خون هستند، ويسکوزيته پايينتري دارند و بهراحتي شسته ميشوند.
در نهايت انحلالپذيري در آب يک عامل بسيار مهم در قابليت پاکسازي اوليه است و آلودگي آزمايشي انتخاب شده، بايد چالش مناسبي براي وسيله ايجاد کند. از آنجا که بسياري از آلودگيهاي بهدست آمده از ترشحات و مايعات بدن بيمار (مانند خون، ادرار و ترشحات مخاطي) قابليت انحلالپذيري در آب را دارند، آب يک حلال جهاني موثر است که در پاکسازي ابزار پزشکي نيز استفاده ميشود. مواد شوينده به فرآيند اضافه ميشوند تا به طرز خاصي اجزاي انحلالناپذير آلودگيهاي باليني (مانند چربيها و … ) را هدف قرار دهند؛ با اين وجود، انحلالپذيري در آب بهعنوان يکي از ويژگي-هاي آلودگي آزمايشي پيشنهاد شده که مبناي ارزشمندي را فراهم ميکند که نشان ميدهد که چگونه اجزاي موجود در آلودگي آزمايشي، در مقايسه با آلودگي واقعي عمل ميکنند.
ترکيب اجزاي مورد استفاده براي يک دستورالعمل آلودگي آزمايشي مصنوعي بايد از نظر فيزيکي بهنحوي عمل کند که چالش مناسبي را براي يک وسيله پزشکي نشان دهد و حاوي اجزاي شيميايي باشد که موفقيت يک فرآيند پاکسازي مؤثر را نشان دهد. دستورالعمل آلودگي بايد همچنين يک چالش پايدار و قابل تکرار را براي فرآيند پاکسازي ايجاد کند. در يک آزمايش، آلودگيهاي آزمايشي براي ابزار جراحي مقايسه شدند و پيشنهاد شد که هنگام انتخاب آلودگي آزمايشي، غلظت پروتئين بهعنوان بخش مهمي از اجزاي آلودگي يافتشده روي ابزارهاي حاوي پروتئين، يک فاکتور کليدي است. در دماهاي بالا، پروتئين تغيير ماهيت ميدهد و سبب افزايش دشواري برداشتن آن ميشود که يک چالش مهم پاکسازي است. ارزيابي ابزارها پس از اعمال جراحي نشان ميدهد که ابزارهاي ارتوپدي و جراحي، بالاترين ميانگين غلظت پروتئين باقيمانده را پس از عملهاي جراحي دارند. براساس اين يافتهها، مقايسه معناداري ميتواند بين غلظت پروتئين در يک آلودگي آزمايشي و ابزار جراحي واقعي وجود داشته باشد.
هدف از اين مطالعه، ارزيابي چهار آلودگي آزمايشي بود که توسط استانداردهاي ISO و ASTM براي جراحي عمومي و ارتوپدي، با استفاده از غلظت پروتئين، ويسکوزيته، چسبندگي و انحلالپذيري در آب مشخص شده است تا تعيين شود که کدام آلودگي آزمايشي براي اعتبارسنجي پاکسازي ابزارهاي ارتوپدي و جراحي از همه مناسبتر است؟
مواد و روشها
انتخاب و آمادهسازي آلودگي. چهار آلودگي آزمايشي توسط استانداردهاي ISO و ASTM مشخص شده تا آلودگي ابزارهاي ارتوپدي و ديگر ابزارها ، پس از آنکه در جراحيها استفاده شدند را شبيهسازي کند. (جدول 2). براي آزمايش از دو جايگزين ابزار استفاده شد. يک قطعه فولاد ضد زنگ به اندازه 10 سانتيمتر مربع، بدون ويژگيهاي ابزارها، براي ارزيابي متغيرهاي آزمايش استفاده شد، درحاليکه کلامپ هموستاز از جنس فولاد ضدزنگ براي ارزيابي عملکرد آلودگي در حضور ويژگيهاي ابزارها (مانند لولاهاي قفل شونده و مفصل محوري) استفاده شد. ابزارهاي جايگزين يا انديکاتور (PCDs) بيشتر هنگام مقايسه متغيرهاي آزمون اعتبارسنجي پاکسازي و قطعات براي مقايسه کلي استيل ضدزنگ استفاده ميشود و کلامپهاي هموستاز براي ارزيابي پيچيدگي ويژگي ابزار بهکار ميروند که بهعنوان يک روش مناسب براي فهم تناسب ابزارهاي جراحي و ارتوپدي ايجاد شدهاند.
■ ويسکوزيته. ويسکوزيته آلودگيها با استفاده از پر کردن توپ ويسکومر (گيلمونت با شماره قطعه GV-2300) بلافاصله پس از آمادهسازي آلودگي، اندازهگيري ميشود. لوله شيشهاي ويسکومر با 5 ميليليتر آلودگي پر ميشود (بدون ذرات معلق) و پس از آن يک توپ از جنس فولاد ضدزنگ (ابزار گيلمونت با شماره قطعه GV-2119S) اضافه ميشود که طي کردن فاصله بين دو خط روي ويسکومر زمانبندي شده بود. آزمايش با سه برابر کردن غلظت آلودگي تکميل شد که با وزن کردن يک ميليليتر از آن و قرار دادن در فرمول زير محاسبه شد.
D=M/V
D غلظت براساس گرم بر ميليليتر، M جرم و V حجم است.
ويسکوزيته با فرمول زير که مختص دستورالعمل کاربردي ويسکومتر توپي گيلمونت است محاسبه شد:
µ=κ(ρfρ)t
µ معادل ويسکوزيته، ρf معادل چگالي توپ 8.02 گرم بر ميليليتر، ρ معادل چگالي آلودگي (گرم بر ميليليتر)، t زمان (ثانيه) و k محتويات ويسکومر (35) است.
■ چسبندگي. سه قطعه در هر آلودگي ارزيابي شد. بلافاصله پس از آمادهسازي، يک ميليليتر از آلودگي روي قطعه فولاد ضدزنگ (10cm × 10cm) اضافه شد و با استفاده از يک پخش کننده شيشهاي، به صورت يکنواخت پخش شد. آلودگي براي مدت حداقل 12 ساعت يا تا زماني که تحت شرايط محيطي کاملا خشک شود، در يک قفسه خشککن نگهداري شد. فرآيند آزمون چسبندگي، همانطور که در نوار تست ASTMD3359-19 توصيف شده، انجام شد و نمونههاي آزمايش، براي مطابقت با طبقهبندي جدول نتايج تست چسبندگي، نگهداري شد.
■ انحلالپذيري در آب. آزمايش انحلالپذيري، روي دو سطح آزمايش انجام شد (تصوير1). يک قطعه فولاد ضدزنگ (10cm × 10cm)، نمونه با اندازه 4 براي نمايش بصري باقيمانده آلودگي و يک کلامپ هموستاز از جنس فولاد ضدزنگ نمونه اندازه 7 براي بررسي کمي باقيمانده آلودگي (براساس وزن) استفاده شد. اندازهگيري وزن براي محاسبه کاهش درصد پروتئينهاي نامحلول و ذرات معلق که ممکن است به کمک سنجشهاي تحليلي پروتئين قابل کشف نباشد، استفاده شد. در ابتدا، همه سطوح آزمايش وزن شد و سپس آلودگي قرار گرفت. قطعات با اضافه کردن يک ميليليتر از آلودگي و پخش يکنواخت آن روي سطح با استفاده از پخشکننده شيشهاي آلوده شدند.
تصوير1: مثالهاي قطعات آزمايش و کلامپهاي هموستاز آلوده شده با ادينبرگ که براي تست انحلالپذيري در آب متعاقب آلودگي استفاده شد (شکل B) و خارجسازي (شکل A) شماره 1، 15 دقيقه غوطهوري، شماره 2، 30 دقيقه غوطهوري و شمارههاي 7-3، 60 دقيقه غوطهوري.
A
B
تصوير2: چسبندگي خون لختهشده با بزرگنمايي 1 برابر
هموستاتها بهطور انفرادي و در حالت باز در آلودگي فرو رفتند و کاملا غوطهور شدند. نمونههاي آزمايش در طول 12 ساعت يا تا زمان خشک شدن کامل، تحت شرايط محيطي در محفظه خشککن خشک شدند و ذرات سست آلودگي با يک دستمال به آرامي پاک شدند تا وزن کلي آلودگي بهکار رفته، بهدست آيد. سپس هريک از نمونهها به کيسههاي منفرد آب مقطر اضافه شدند تا کاملا غوطهور شوند (هموستات در حالت باز شده). نمونههاي آزمايش به ترتيب براي 15، 30 و 60 دقيقه در يک حمام آب گرم (45 درجه سانتيگراد) شناور شدند. پس از برداشتن از حمام آب، پيش از وزن کردن مجدد به منظور تعيين درصد آلودگي برداشته شده، به نمونهها اجازه داده شد تا براي مدت حداقل 12 ساعت خشک شوند.
درصد پروتئين. هر آلودگي آزمايشي بايد براي متوسط غلظت پروتئين ارزيابي شود. براي هر آلودگي 5 واحد 0.5 ميليليتري آلودگي به 50 ميليليتر معرف استريل ACS اضافه و مخلوط شد. غلظت پروتئين با استفاده از معيار برادفورد براي غلظت پروتئين محاسبه شد.
نتايج
■ ويسکوزيته. ترکيب آلودگي ادينبرگ بالاترين ويسکوزيته را نشان داد (>1000 Cp) و به دليل وجود غلظت زياد و ذرات ريز، نميتوان ويسکوزيته دقيق را با استفاده از روش توصيفشده، تعيين کرد. بهطور مشابه، ويسکوزيته خون لخته شده نيز نميتواند تعيين شود. فرآيند لخته شدن آلودگي تقريبا به 10-15 دقيقه زمان نياز دارد تا تکميل شود. به منظور بهدست آوردن نتيجه ويسکوزيته اوليه، خون 5 دقيقه پس از پروتامين سولفات به سيستم آزمايش وارد شد. براساس اين آناليز، بهطور کلي آلودگي اصلاح شده خون لخته شده، بالاترين ويسکوزيته اندازهگيري شده را نشان داد و پس از آن به ترتيب DBLSO و خون لخته شده قرار داشت (تصوير3).
تصوير3: متوسط ويسکوزيته آلودگي آزمايشي
توجه: ويسکوزيته آلودگي ادينبرگ ( cp1000< ) ميتوانست تعيين شود و هر دو آلودگي آزمايشي لخته شده قبل از لخته شدن آزمايش شد.
■ چسبندگي. چسبندگي به منظور توانايي برداشتن آلودگي از روي سطح، آزمايش شد. تنها آلودگي آزمايشي که نتايج تکراري براي تست چسبندگي نشان داد، خون لخته بود که به ميزان پايدار 90٪ برداشت آلودگي دستيافت (تصوير2). نتايج در تصوير 4 خلاصه شدهاند.
تصوير4: نتايج روش چسبندگي با استفاده از نوار تست ASTM D3359-19 براي چسبندگي
■ انحلالپذيري در آب. براي هر آلودگي، درصد آلودگي برداشتشده، در فواصل 15، 30 و 60 دقيقه محاسبه شد. بين فواصل زماني هيچ تفاوت آماري مشاهده نشد (تصوير5).
تصوير5: نتايج انحلالپذيري در آب در همه فواصل زماني
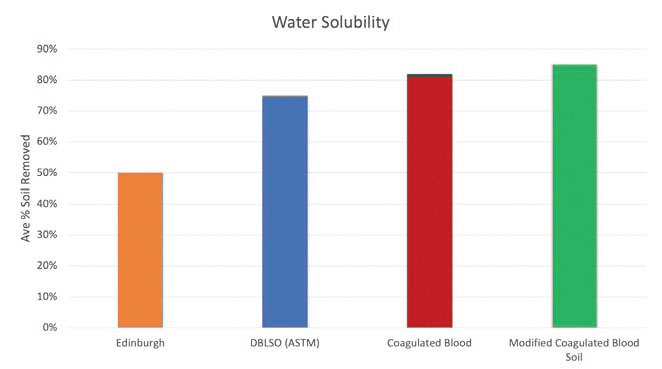
براي مقايسه عملکرد آلودگي آزمايشي، بزرگترين فاصله زماني، يعني 60 دقيقه استفاده شد (تصوير6). آلودگي ادينبرگ پايينترين انحلالپذيري در آب را نشان داد و پس از آن به ترتيب DBLSO، خون لخته و آلودگي اصلاحشده خون لخته قرار داشت. آلودگي ادينبرگ، DBLSO و آلودگي اصلاحشده خون لخته بهترين تکرارپذيري را با 6-4٪ تغيير نشان دادند، درحاليکه خون لخته 19٪ تغيير را نشان داد. نتايج در تصوير 6 خلاصه شدهاند.
تصوير 6: مقايسه انحلالپذيري در آب آلودگي آزمايشي در زمان 60 دقيقه خارجسازي
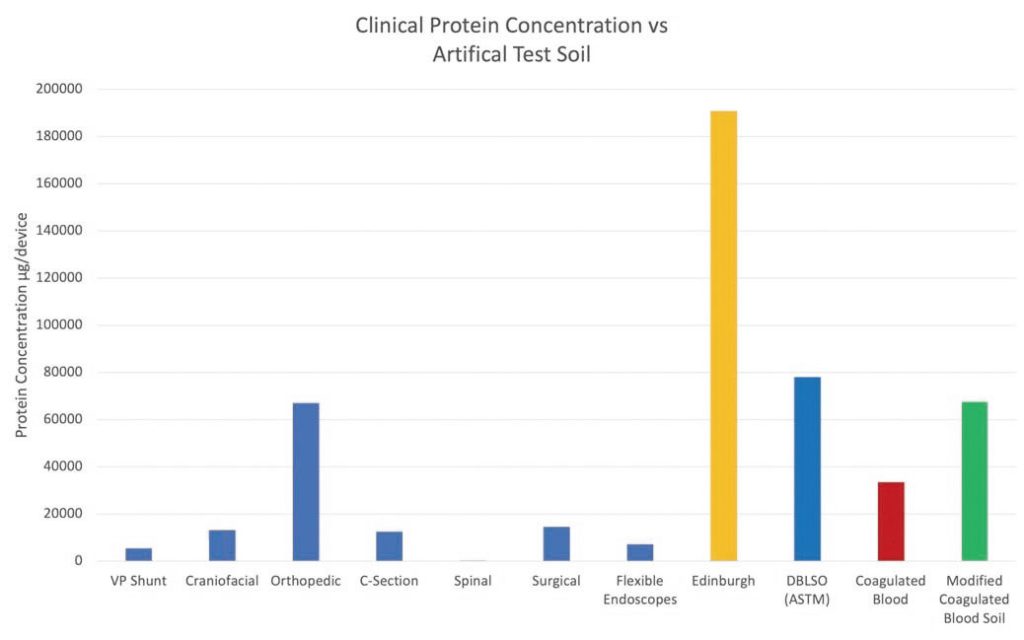
■ غلظت پروتئين. غلظت پروتئين آلودگيها به ترتيب براساس ميکروگرم بر ميليليتر تعيين شد. آلودگي اصلاحشده خون لخته، بالاترين ميانگين غلظت پروتئين را داشت (160000 ميکروگرم بر ميليليتر)، DBLSO و آلودگي خون لختهشده غلظتهاي مشابهي داشتند (140000 ميکروگرم بر ميليليتر) و آلودگي ادينبرگ پايينترين غلظت را داشت (110000 ميکروگرم بر ميليليتر). با استفاده از چگالي آلودگي که در در آزمايش ويسکوزيته محاسبه شد، نتايج مجددا براساس ميکروگرم گزارش و به يک دستگاه داده شد (با استفاده از مقاله جايگزين آزمايش هموستات) تا همانطور که در تصوير 7 نشان داده شده است، با غلظتهاي پروتئين موجود روي ابزارهاي جراحي، پس از استفاده روي بيمار مقايسه شود. با استفاده از اين محاسبه، ادينبرگ بالاترين غلظت پروتئين را نشان داد، DBLSO و آلودگي اصلاحشده خون لخته پايينترين ميزان را داشت (تصوير7). سطوح پروتئين گزارش شده براي ابزار جراحي ارتوپدي (معادل 60000 ميليگرم در هر وسيله)، بدترين مورد بود و سطوح پروتئين يافت شده در DBLSO و آلودگي اصلاحشده خون لخته يکسان بود.
تصوير7: مقايسه غلظتهاي پروتئين (بر اساس ميليگرم در هر وسيله) از اعمال جراحي در مقابل چهار آلودگي آزمايشي
بحث
هنگام انتخاب يک آلودگي آزمايشي مرتبط، براي مطالعه اثربخشي پاکسازي، اولين ملاحظه بايد تماس با بيمار و نحوه کار وسيله باشد. آلودگيها بايد بدترين نوع چالش را براي فرآيند پاکسازي ايجاد کنند و تا آنجا که ممکن است ويژگيهاي آلودگيهايي را که وسايل، طي استفاده باليني با آنها در تماس هستند را تکرار کنند. اين انتظار وجود دارد که آلودگي آزمايشي، به سطح وسيله متصل ميشود و آنچنان به درون بخشهاي مختلف وسيله جريان مييابد که ممکن است با بهکار بردن مستقيم آلودگي، بهراحتي قابل دسترس نباشد (شبيهسازي جريان خون يا مايع، طي استفاده). همچنين، اين ملاحظه بايد تکرارپذيري عملکرد آلودگي با اجزايي که دائما بهکار ميروند را درنظر گيرد و عناصر باليني قابل اندازهگيري را ايجاد کند که نشاندهنده استفاده باليني باشد (مانند پروتئينها، چربيها، کربوهيدراتها و غيره).
تمام آلودگيهاي آزمايششده، سطح مورد انتظار و قابلقبولي از تنوع را نشان دادند. آلودگيها، غلظتهاي تکرارپذيري از پروتئين را نشان دادند که کمتر از 10٪ بود، به استثناي آلودگي ادينبرگ که تغيير 19 درصدي داشت. اين امر ممکن است تنوع طبيعي در منابع مختلف غلظتهاي آلودگي (مانند خون و تخممرغ) و داشتن غلظتهاي کنترلنشدهاي از پروتئين، کربوهيدرات و چربي باشد. همانطور که در مطالعات ديگر اشاره شده است، آلودگي زرده تخممرغ از همه سختتر پاک ميشود، زيرا آنها حاوي اسيدهاي آمينه (پروتئين) هستند که در اثر گرما و خشک شدن، از حالت آبدوست به آبگريز تغيير ميکنند. اين تغيير باعث ميشود که پروتئينها به سطوح متصل شوند و هنگام پاکسازي وسيله، برداشتن آنها بسيار سخت باشد. اين مفهوم، توسط نتايج تست چسبندگي نشان داده شد که در آن، فقط خون لخته شده(يعني تنها آلودگي آزمايشي بررسي شده در اين مطالعه که حاوي تخممرغ در اجزاي خود نبود) بود که همواره پس از خشک شدن برداشته ميشود. در ادامه، با بهکار بردن آلودگي، تأثير آلودگي شيميايي مشاهده شد. هنگام آلوده کردن سطح قطعات فولاد ضدزنگ با خون لخته شده، اگر خون قبل از شروع فرآيند لخته شدن، استفاده نشود، لخته خون سفتشده باعث ميشود که ابزارها ميزان برابري از آلودگي آزمايشي را دريافت نکنند. بنابراين، گرچه ويسکوزيته پايين خون، قبل از لخته شدن، ظرفيت نفوذ بالاتري ايجاد ميکند، بهموقع بودن استفاده از آلودگي، براي ايجاد چسبندگي، حياتي است. همانطور که با خون لخته شده اصلاحي نشان داده شده است، اجزاي ديگر موجود در يک آلودگي آزمايشي، ممکن است ويژگي فيزيکي مهمي را ايجاد کنند که به فيبرين اجازه ميدهد تا پروتوفيبريلهاي دو رشتهاي که بهصورت جانبي در حال تجمع هستند، الياف شاخهاي تشکيلدهنده يک شبکه سهبعدي را ايجاد کنند، يعني شرايط مناسب براي افزايش سرعت تبديل خون به يک ماده ويسکوالاستيک محکم و چسبيدن به مواد مختلف.
ارزيابي نشانگر زيستي ابزارهاي باليني، نشان ميدهد که ابزارهاي ارتوپدي و جراحي، بالاترين سطوح پروتئين باقيمانده را پس از استفاده روي بيمار دارند. از آنجا که پروتئين، نشانگر زيستي اوليه است که بهعنوان شاخص نشاندهنده نقاط پاياني پاکسازي عمل ميکند، غلظت پروتئين در آلودگيهاي آزمايشي بايد نشاندهنده سطوح مشاهده شده هنگام استفاده وسيله، روي بيمار باشد. هنگام مقايسه با غلظتهاي باليني مشاهده شده روي ابزارها، پس از استفاده روي بيمار، مشخص شد که آلودگي ادينبرگ که غلظت پروتئين آن 3 برابر بالاتر از موارد گزارش شده در اقدامات باليني است، چالش بزرگتري را ايجاد ميکند. DBLSO و BLSO، از نظر غلظت پروتئين برابري بيشتري داشتند و چالش مناسبتري براي انواع ابزارها ايجاد ميکنند. سطوح خون لخته شده نشان ميدهد که ممکن است براي ابزارهاي جراحي، آلودگي مناسبي باشد، اما براي ابزارهاي ارتوپدي مناسب نيست.
تکنيک استفاده از آلودگي آزمايشي براي يک وسيله، بايد بدترين شرايط باليني را شبيهسازي کند. اجزاي وسيله و شبيهسازي کارکرد آن، ميتواند روي نتيجه تستهاي اثربخشي پاکسازي تأثير بگذارد. آلودگيهاي آزمايشي بايد ويسکوزيته مناسبي داشته باشند تا بتوانند اجزاي وسيله (مانند مجاري، دريچهها، شکافها، لولاها و مفاصل، سطوح خشن و نامنظم و قسمتهاي داخلي متحرک) را که احتمال بيشتري براي تجمع و حفظ آلودگي دارند، به چالش بکشند. ممکن است استفاده از شبيهسازيها تحت شرايط آزمايشگاهي، هميشه کاربرد باليني را تکرار نکند. آلودگيهاي آزمايشي بايد قادر به نفوذ به داخل قسمتهاي چالش برانگيز وسيله باشند و ويسکوزيته آلودگي ممکن است مانع اين امر شود. ناتواني در اندازهگيري ويسکوزيته آلودگي ادينبرگ نشان ميدهد که احتمالا اين نوع آلودگي، ويسکوزيته مناسبي را براي به چالش کشيدن قسمتهاي بحراني ابزار ندارد. با اينحال، تست ناموفق ويسکوزيته براي خون لخته نشان ميدهد که استفاده فوري براي رسيدن به جريان و ظرفيت نفوذ دلخواه، ضروري است.
خشک کردن و استفاده از گرما (مانند سوزاندن) ميتواند روي خواص شيميايي آلودگي تأثير بگذارد، لذا درصورتيکه وسيله مورد نظر، هنگام استفاده، اين شرايط را تجربه ميکند، بايد شبيهسازي مناسب صورت گيرد. درک تأثير رقيقسازي آلودگي با يک رقيقکننده خاص، در طول عملهاي جراحي (مانند ويسکوالاستيک طي جراحي چشم) ميتواند مهم باشد تا اين شرايط را طي تستهاي تأييدي، شبيهسازي کند.
در مجموع، هنگام انتخاب يک آلودگي آزمايشي، عملکرد آلودگي بايد با در نظر گرفتن شبيهسازي کاربرد باليني، چسبندگي، ويسکوزيته، غلظتهاي شناساگر (مانند پروتئين) و تکرارپذيري ارزيابي شود. اين مطالعه نشان داد که ممکن است فرمولاسيون آلودگي ادينبرگ، بهطور کامل مرتبط با آلودگيهاي باليني براي ابزار پزشکي نباشد. ممکن است ويسکوزيته چالش مناسبي را براي وسايل با ويژگيهاي پيچيده نشان ندهد و غلظت پروتئين نسبت به ارتباط باليني، چالش برانگيزتر باشد. به طرز مشابه، دادههاي چسبندگي آلودگي و غلظت پروتئين نشان ميدهند که ممکن است خون لخته شده چالش مناسبي براي اندازهگيري اثربخشي پاکسازي، در همه ابزارهاي پزشکي (مانند ارتوپدي) ارائه ندهد.
هنگام ايجاد تکرارپذيري در اين آلودگي آزمايشي، روش بهکار بردن وسيله، يک عامل حياتي خواهد بود و زمان لخته شدن بايد به خوبي کنترل شود تا از آلودهسازي مناسب مطمئن شويم. اضافه کردن خون لخته به دستورالعمل DBLSO به اين دليل انجام شد تا بفهميم که چگونه فيبرين، يک پروتئين غيرکروي موجود در خون، هنگام ترکيب شدن با اجزاي پيچيده ديگر مانند زرده تخممرغ روي ويژگيهاي آلودگي تأثير ميگذارد. هنگام انجام تستهاي انحلالپذيري در آب ، در زمان استفاده از خون لخته شده (با فرض فيبرين) و همچنين DBLSO، باقيمانده مواد پروتئيني مشاهده شد (تصوير 8). اين دادهها نشان ميدهند که حداقل، انحلالپذيري DBLSO به اندازه خون لخته شده است و خون لخته شده اصلاحي ممکن است از ديدگاه پاکسازي، چالشهاي بيشتري را ارائه دهد (به دليل حضور پروتئينهاي نامحلول در آب).
دادههاي ارائه شده در اين مطالعه نشان ميدهد که آلودگي خون بدون فيبرين، يک آلودگي آزمايشي مناسب براي به چالش کشيدن ابزار جراحي (شامل آنهايي که در ارتوپدي استفاده ميشوند) است. فرمولاسيون اين آلودگي ممکن است بافت نرم، مخاط، خون در گردش، استخوان/مغز استخوان و مايع نخاعي را به اندازه کافي نشان دهد تا اين ابزارها را به طرز مناسبي به چالش بکشد. ويسکوزيته آلودگي، همانطور که در مورد آناليز انحلالپذيري در آب يا غلظت پروتئين نشان داده شده است اجازه بهکار رفتن آن را در شرايط هندسي پيچيده و چسبندگي مواد ميدهد. اين آلودگي، بهترين ترکيب از متغيرهاي آلودگي آزمايشي تست شده در اين مطالعه را دارد و ميتواند چالش مناسبي را براي نشان دادن اثربخشي استريل شدن ابزار جراحي چندبار مصرف ارائه دهد.
تصوير 8: مثالهاي باقيماندههاي پروتئين (نامحلول در آب) از آلودگيهاي آزمايشي خون لخته شده (1) و DBLSO (2) با بزرگنمايي يک برابر